с 01.01.2013 по настоящее время
Россия
В статье представлена модифицированная имитационная SEIR-модель распространения эпидемии. Предложенная модель реализована в системе AnyLogic. Данная модель позволяет провести оценку ограничительных мероприятий, направленных на снижение роста эпидемии. Представлены результаты расчетов по четырем основным сценариям: 1) Без ограничительных мероприятий; 2) При мягких ограничительных мерах; 3) В условиях жестких ограничительных мер, но носящих рекомендательный характер; 4) При введении полного карантина и объявлении чрезвычайной ситуации. Результаты позволяют спрогнозировать примерные даты пика эпидемии, окончания эпидемии, количество умерших и нагрузку на систему здравоохранения при каждом из сценариев для двух городов (Москва и Санкт-Петербург).
эпидемия, имитационное моделирование, модель, AnyLogic, COVID-19, сценарии развития, управленческие решения, ограничительные мероприятия, чрезвычайная ситуация
Введение
В настоящее время в условиях эпидемии в результате распространения коронавируса SARS-Cov-2 (COVID-19) и де-факто наступившей биолого-социальной чрезвычайной ситуации стоит задача прогнозирования размеров потенциального социального ущерба, сроков пика и окончания распространения эпидемии, а также оценки эффективности возможных управленческих решений, направленных на предотвращение распространения эпидемии.
На помощь в этом случае могут прийти математические модели, описывающие данные процессы. И к настоящему времени существует несколько подходов к моделированию распространения эпидемии, которые могут быть использованы для анализа протекающих процессов и сравнения альтернативных путей развития в зависимости от принятых управленческих решений.
Анализ моделей
Самой простейшей является SIR-модель (Susceptible–Infected–Removed model), в которой каждый из индивидуумов, входящих в исследуемую популяцию, может находиться в одном из трех возможных состояний: Susceptible (потенциально восприимчивый к заражению), Infected (инфицированный), Removed (выздоровевший и невосприимчивый к заражению). Предполагается, что индивидуумы могут стать невосприимчивыми к заражению только после полного извлечения от инфекции, т.е. в какие-то моменты времени для каждого возможна последовательность переходов Susceptible ® Infected ® Removed.
Основными базовыми предположениями при использовании данной модели является следующие:
– каждый из восприимчивых индивидуумов, контактирующий с инфицированным, имеет определенную вероятность заражения, независящую от времени;
– скорость заражения пропорциональная количеству инфицированных индивидуумов, а также количеству восприимчивых (действительно, чем больше у инфицированных среди всех их контактов людей восприимчивых к заражению, тем будет выше скорость заражения, но конечно при неизменном среднем количестве контактов среди всей исследуемой популяции).
– каждый инфицированный, в свою очередь, имеет постоянную вероятность выздоровления в единицу времени;
– скорость выздоровлений пропорциональна количеству инфицированных.
Если в какой-то период времени скорость заражения оказывается выше скорости выздоровлений, это означает, что данный период характеризуется распространением эпидемии. В противном случае, можно будет говорить о том, что эпидемия затухает.
В целом, SIR-модель может позволить, по крайней мере, в первом приближении оценить примерную динамику распространения эпидемии. Но реальный процесс протекания болезней несколько сложнее, необходимо учитывать при моделировании еще ряд факторов. В первую очередь это касается того, что процесс заболевания может состоять как минимум из двух стадий: инкубационный период (без внешних признаков заболевания) и непосредственно период болезни (с наличием внешних признаков заболевания и возможной при этом изоляции инфицированного индивидуума). Кроме того могут заболевание каждого индивидуума может протекать в различных формах: в легкой (когда индивидуум может переносить болезнь в домашних условиях), в средней (с возможной необходимостью госпитализации) и в тяжелой (на примере COVID-19 болезнь может перейти в коронавирусную пневмонию с необходимостью перевода пациентов в реанимационное отделение и применения аппаратов искусственной вентиляции легких).
Учесть первый из данных факторов позволяет SEIR-модель (Susceptible–Exposed–Infected–Removed model), являющаяся некоторой модификацией SIR-модели. В данной модели каждый индивидуум может находиться уже в одном из четырех возможных состояний. К трем рассмотренным состояниям в SIR-модели добавляется еще одно Exposed (зараженный, находящийся в инкубационном периоде). В какие-то моменты времени для каждого возможна последовательность переходов Susceptible ® Exposed ® Infected ® Removed.
Реализовать данную модель можно как с применением аналитического (с составлением системы дифференциальных уравнений), так и имитационного моделирования. С учетом того, что требуется рассмотрение различных сценариев, в которых могут учитываться определенные внешние воздействия на систему, отражающие какие-то профилактические или ограничительные мероприятия, некоторые из параметров данной системы (например, частота социальных контактов) будут нестационарными. Кроме того, анализ распространения и тяжести протекания болезни при СOVID-19 за прошедший период, предполагает необходимость разделения всей исследуемой популяции на некоторые возрастные категории, т.к. по большей части у молодого населения болезнь протекала в легкой стадии. В то же время, у старшего населения очень часто болезнь протекала в тяжелой форме и заканчивалась зачастую летальным исходом.
Данные обстоятельства значительно усложняют построение аналитической модели и для реализации был выбран метод имитационного моделирования.
Имитационная модель
Предлагаемая имитационная модель разработана в среде AnyLogic и основана на SEIR-модели, но определенным образом модифицирована с учетом некоторых особенностей, присущих именно эпидемии COVID-19:
1. Инкубационный период был разделен на две фазы, поэтому состояние Exposed было разделено на два других. В первой фазе (латентный период) индивидуум уже является носителем инфекции, но отсутствуют внешние проявления инфекции, и индивидуум не опасен для окружающих, т.е. отсутствует потенциальная способность к их заражению. Во второй фазе зараженный уже проявляет внешние признаки имеющейся инфекции, способен заражать окружающих, но еще не идентифицирован системой здравоохранения, т.е. не попал в официальную статистику инфицированных. Именно на данной стадии и происходит фактически процесс распространения эпидемии. Введение двух состояний позволяет учесть как раз те особенности при распространении COVID-19, когда далеко не все инфицированные сразу обращаются в медицинские службы, существуют ограничения на проведение тестирования на вирус, как по их количеству, так и по времени получения результатов.
2. В интересах оценки потребности системы здравоохранения в койко-местах для лечения тяжело инфицированных, а также количества мест в реанимационных отделениях, оснащенных аппаратами искусственной вентиляции легких (ИВЛ), все инфицированные разделяются на три категории: переносящие вирус в легкой форме (без госпитализации), в тяжелой форме (с госпитализацией), а также находящиеся в критическом состоянии (с использованием аппаратов ИВЛ и помещением в реанимационное отделение).
3. Все лица, попавшие в категорию инфицированные (Infected), попадают в карантин и у них практически отсутствуют социальные контакты, т.е. они не могут уже заражать окружающих.
4. При распространении эпидемии нас, естественно, еще будет интересовать и смертность населения в результате COVID-19, поэтому вводится еще одно состояние Dead (умершие).
Основные параметры, включенные в данную модель:
TotalPopulation – численность населения;
ContactRateInfectious – среднее количество социальных контактов у одного человека в день;
ProbInfec – вероятность инфицирования человека в результате его контакта с уже заразившимся;
AvarIncubTime_NonСontagious – средний инкубационный период, в течение которого у заразившегося отсутствует потенциальная способность к их заражению окружающих;
AvarIncubTime_Сontagious – средний инкубационный период, когда инфицированный уже может заражать окружающий, до момента его социальной изоляции;
ProportionCritical – доля тяжело больных, которым необходима госпитализация;
ProportionHard – доля критически больных, помещаемых в реанимационное отделение с аппаратами ИВЛ;
ProbDeath – вероятность смерти лиц, находящихся в реанимационном отделении;
AvarageIllnessPeriod – средняя длительность болезни (не включая инкубационный период), переносящих ее в легкой форме;
AvarageHospitalTime – среднее время лечение тяжело больных, находящихся в стационаре.
Реализованная системно-динамическая модель распространения эпидемии представлена на рис.1.
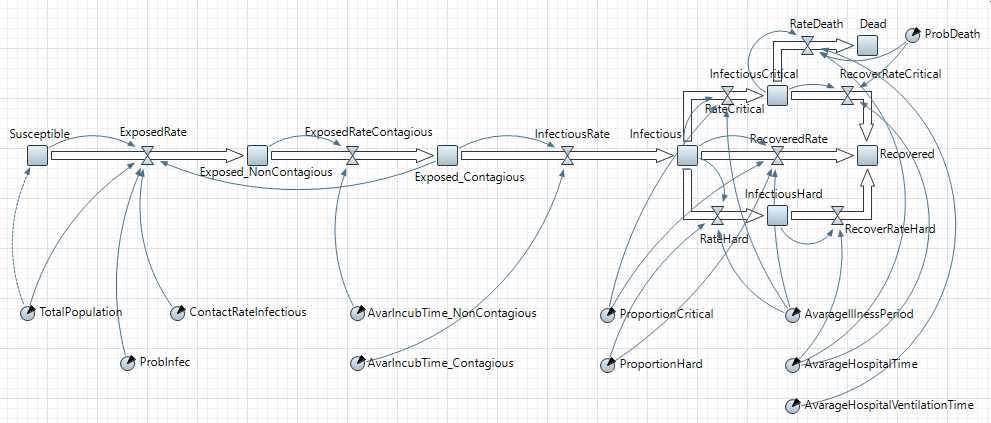
Рисунок 1 – Модель распространения эпидемии
Оценка исходных параметров для моделирования
Адекватность полученных результатов при использовании разработанной модели распространения эпидемии определяется, в том числе, и адекватностью исходных параметров, которые необходимо подать на вход модели. Необходимо учитывать, что некоторые параметры имеют определенные региональные особенности (которые могут зависеть, например, от плотности населения), а некоторые характерны именно для данного вируса, и по этой причине необходимо провести анализ результатов исследований вирусологов или практикующих медиков.
Официальные данные Всемирной организации здравоохранения (ВОЗ) говорят об инкубационном периоде, составляющем от 2 до 14 дней [1]. Исследования ученых-вирусологов также показали, что инкубационный период у разных пациентов может достаточно сильно отличаться, но в среднем его латентный период составляет около 5.2 дней, а период, когда инфицированный уже заразен и может инфицировать окружающих до того как попадает в официальную статистику и фактически изолируется, составляет порядка 3 дней [2-5]. Именно данные значения приняты в качестве исходных в модели.
По данным ВОЗ, которая аккумулирует все информационные потоки по распространению и анализу течения коронавируса «… у 15% пациентов заболевание может проходить в тяжелой форме, требующей кислородной терапии или иного лечения в условиях стационара и примерно 5% случаев – это критическая степень тяжести заболевания, при которой требуется искусственная вентиляция легких» [6, 7]. Данные значения мы будем ориентироваться при определении параметров ProportionHard и ProportionCritical. Хотя по данным статистики коронавируса в США 20% нуждаются в госпитализации и все те же 5% из числа заболевших нуждаются в интенсивной терапии, включая использование аппаратов искусственной вентиляции легких (ИВЛ).
При этом характерной особенностью протекания COVID-19 является явно выраженная неоднородность тяжести протекания заболевания и летальности относительно возраста зараженных [8, 9]. Вполне очевидно, что точно определить значение показателя летальности можно будет лишь по окончанию распространения эпидемии, а в настоящее время вспышка вируса еще продолжается. И данный показатель достаточно сильно варьируется в разных странах от 0.4% до 4% от общего числа заболевших [10-11].
В нашей стране данный показатель пока держится на уровне 0.7-0.8%, но совершенно ясно, что данные значения ниже истинной летальности, т.к. пик эпидемии еще не пройден, а смертельные случаи наступают значительно позже выявления заражения. Мы будем ориентироваться на значение летальности около 1%, хотя оно может и не отражать реальной картины.
При легкой форме заболевания и отсутствии осложнений период болезни оценивается в 7-10 дней [12]. Поэтому в модели значение показателя AvarageIllnessPeriod принималось равным 7 дням. Оценки периода нахождения больных в стационаре и реанимационном отделении представлены в работе [13], где данные периоды оказались одинаковыми и также равны 7 дням. Однако, учитывая официально представленную статистику по динамике выздоровления в нашей стране, видно, что данные значения являются весьма оптимистическими и далеко не совсем соответствуют реальной ситуации. Данный период оценивается не менее 10 дней [14].
При анализе эпидемии SARS-Cov-2 специалистами ВОЗ установлено, что базовое репродуктивное число (то есть среднее количество заражаемых лиц от одного больного) колеблется от 1.4 до 2.5, что меньше аналогичных показателей при ОРВИ (от 2 до 5) [15, 16].
Однако данные значения могут существенно отличаться для различных регионов. Совершенно неправильным будет использовать одни и те же значения, к примеру, для мегаполисов и малых городов.
Значения данного параметра (а он формируется под воздействием ContactRateInfectious и ProbInfec) достаточно проблематично определить напрямую. Но с учетом того, что у нас уже есть реальные данные о распространении эпидемии во многих регионах, то можно определить данные параметры, проводя эксперименты с уже готовой имитационной моделью, и осуществляя калибровку параметров таким образом, чтобы результаты, полученные при моделировании, максимально точно соответствовали реальным ретроспективным данным. Использовался интегрированный в AnyLogic оптимизатор OptQuest, разработанный компанией OptTek System, Inc [17].
В данной работе проводятся исследования распространения COVID-19 на территории двух городов – Москвы и Санкт-Петербурга, поэтому данные параметры отдельно исследуются для каждого из рассматриваемых городов.
Так, результаты калибровки данных параметров для г. Москва показали, что в период с 5 марта по 29 марта на первом этапе распространения эпидемии до введения ограничительных мероприятий ContactRateInfectious = 6,97 и ProbInfec = 0,182.
Анализ полученных результатов использования модели при данных входных параметрах показывает, что они вполне отражают реальную динамику распространения эпидемии на территории г. Москва (см. рис.2).
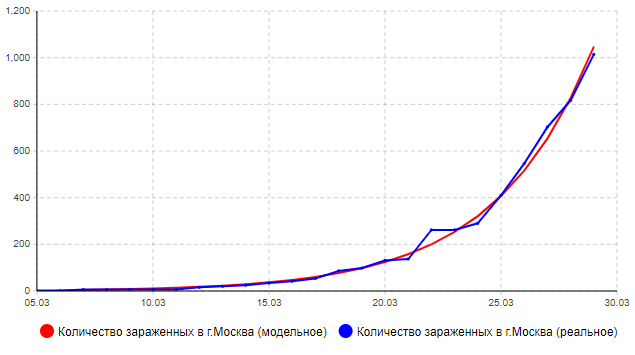
Рисунок 2 – Динамика распространения COVID-19 на территории г. Москва в период 5марта – 29 марта
С 17 марта были введены ограничительные мероприятия, которые естественным образом привели к снижению количества социальных контактов. Аналогичным образом была проведена калибровка параметров и получено, что в условиях введенных мер ContactRateInfectious = 6,2, т.е. количество социальных контактов в целом уменьшилось на 11.1%.
С 30 марта был введен режим самоизоляции, что привело к еще большему снижению количества социальных контактов. С учетом имеющихся реальных данных о динамике заражения в период с 30 марта аналогичным образом была проведена калибровка параметров и получено ContactRateInfectious = 2,205 (т.е. среднее количество контактов уменьшилось в среднем на 68.4%) и ProbInfec = 0,103. Уменьшение показателя вероятности инфицирования индивидуума легко объяснимо эффективностью проведения информирования населения об профилактических мерах при распространении эпидемии, соблюдения правил личной и общественной гигиены.
Аналогичным образом была проведена калибровка данных параметров для г. Санкт-Петербург и модель распространения эпидемии с полученными параметрами в течение первого месяца достаточно неплохо отражает реальную ситуацию (см. рис.3).
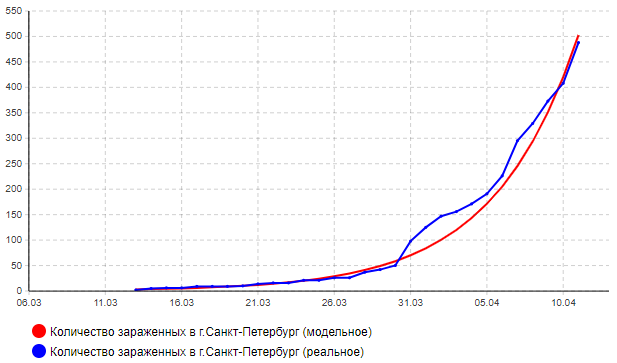
Рисунок 3 – Динамика распространения COVID-19 на территории г. Санкт-Петербург в период 6 марта – 12 апреля
Анализ результатов моделирования
1) г. Москва
Сценарий 1. Распространение эпидемии без каких-либо профилактических и ограничительных мероприятий
Результаты расчетов согласно данному сценарию представлены на рис. 4.
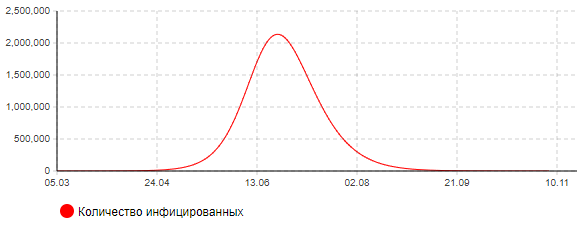
Рисунок 4а – Динамика количества инфицированных (сценарий 1)
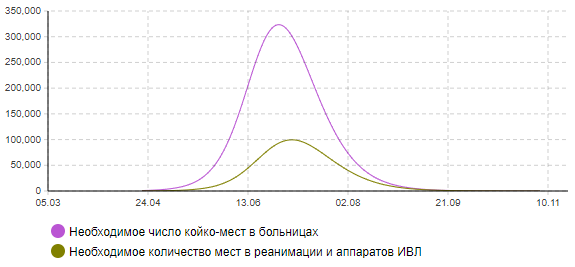
Рисунок 4б – Динамика количества тяжелых и критически больных (сценарий 1)
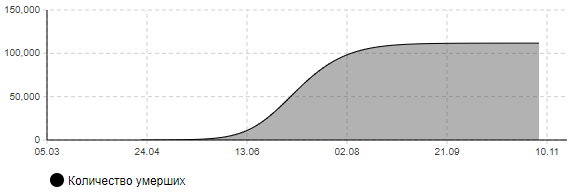
Рисунок 4в – Количество умерших (сценарий 1)
Анализ результатов показывает, что пик эпидемии в этом случае придется на конец июня месяца. Может потребоваться одновременно около 320 тыс. мест в больницах, в том числе 97 тыс. коек в реанимации, оснащенных аппаратами ИВЛ. В целом переболеет 83% населения города. Количество умерших составит около 112 тыс. человек. Окончание эпидемии при данном сценарии ожидается в конце августа.
Вполне очевидно, что такой сценарий изначально был маловероятен, т.к. в любом случае были бы приняты какие-либо ограничительные меры. И результаты вполне отчетливо дают понять о степени потенциальной опасности при распространении эпидемии, а также о необходимости принятия в той или иной степени таких мер. А вот для определения степени ограничений требуется рассмотрение следующих сценариев.
Сценарий 2. Мягкие ограничительные меры
Данные меры были введены на первом этапе борьбы с COVID-19 в России, когда были закрыты образовательные учреждения, отменены мероприятия с массовым пребыванием людей (более 50 человек) и даны рекомендации лицам старшего поколения (после 65 лет) не покидать места их постоянного пребывания (см. рис. 5).
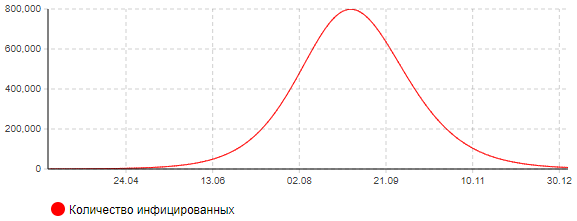
Рисунок 5а – Динамика количества инфицированных (сценарий 2)
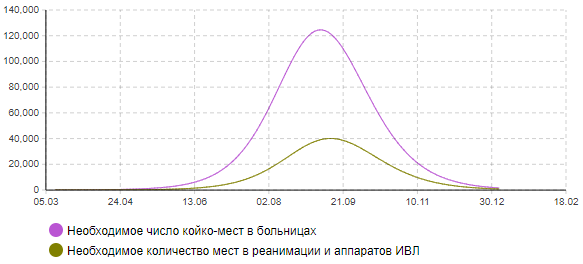
Рисунок 5б – Динамика количества тяжелых и критически больных (сценарий 2)
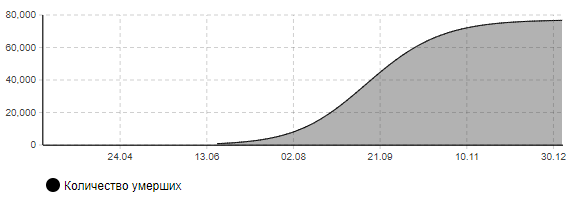
Рисунок 5в – Количество умерших (сценарий 2)
Как видно из представленных результатов, пик эпидемии при данном сценарии придется на начало сентября месяца. Может потребоваться одновременно около 123 тыс. мест в больницах, в том числе 40 тыс. коек в реанимации, оснащенных аппаратами ИВЛ. В целом эпидемия может затронуть 58% населения города. Количество умерших составит около 77 тыс. человек. Окончание эпидемии можно ожидать в конце календарного года.
Сценарий 3. Жесткие ограничительные меры
Данные меры были введены на втором этапе борьбы в нашей стране, когда был объявлен режим самоизоляции для всех граждан, рекомендующий их нахождение в местах постоянного пребывания, за исключением сотрудников, работающих на предприятиях жизнеобеспечения, силовых структур и органов власти. По возможности перевод деятельности бизнеса в дистанционный формат.
Результаты моделирования распространения эпидемии при данном сценарии представлены на рис. 6.
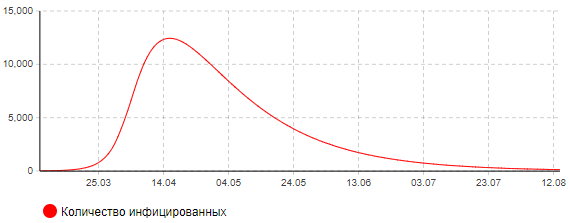
Рисунок 6а – Динамика количества инфицированных (сценарий 3)
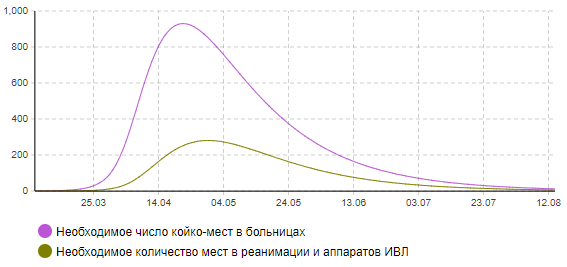
Рисунок 6б – Динамика количества тяжелых и критически больных (сценарий 3)
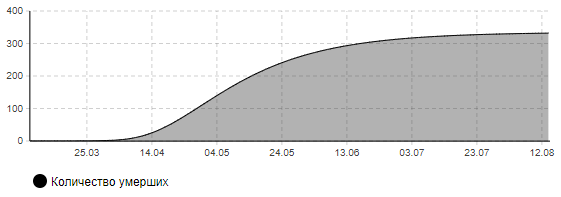
Рисунок 6в – Количество умерших (сценарий 3)
Анализ результатов показывает, что пик эпидемии в этом случае придется на середину апреля. Может потребоваться одновременно около 950 мест в больницах, в том числе 300 коек в реанимации, оснащенных аппаратами ИВЛ. В целом переболеет около 21 тыс. человек. Количество умерших составит около 330 человек. Окончание эпидемии ожидается к началу августа.
Сценарий 4. Жесткие ограничительные меры (введение карантина и режима ЧС)
Данный сценарий подразумевает полный запрет покидания людьми места постоянного пребывания (с введением жестких штрафных санкций, нарушившим режим самоизоляции), организация доступа исключительно в аптеки и магазины, осуществляющие продажу товаров первой необходимости, причем по одному. При данном сценарии также происходит фактически полное временное закрытие бизнесов, за исключением предприятий жизнеобеспечения, ограничение въезда и выезда в отдельные города, остановка пассажирских железнодорожных и авиационных перевозок.
Результаты моделирования распространения эпидемии при данном сценарии представлены на рис. 7.
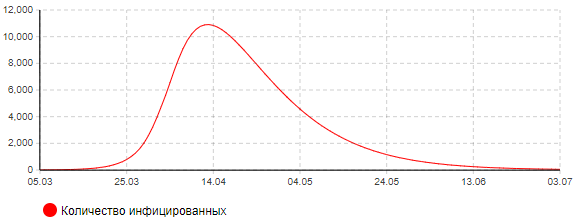
Рисунок 7а – Динамика количества инфицированных (сценарий 4)
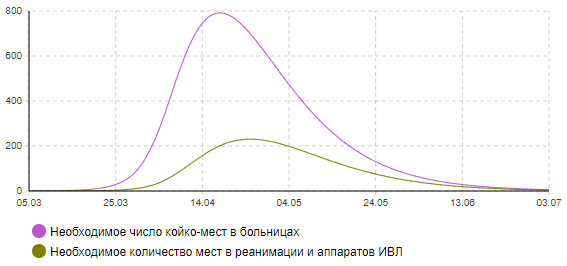
Рисунок 7б – Динамика количества тяжелых и критически больных (сценарий 4)
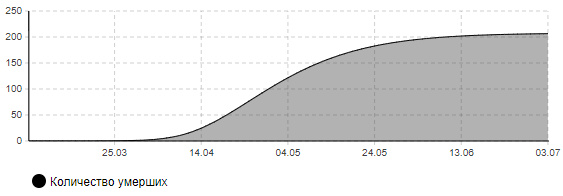
Рисунок 7в – Количество умерших (сценарий 4)
Анализ результатов показывает, что пик эпидемии в этом случае придется на середину апреля. Может потребоваться одновременно около 800 мест в больницах, в том числе 250 коек в реанимации, оснащенных аппаратами ИВЛ. В целом переболеет около 13 тыс. человек. Количество умерших составит около 210 человек. Окончание эпидемии ожидается к середине июня.
Таблица 1.
Оценка эффективности принимаемых мер по распространению COVID-19 в г. Москва
|
|
Сценарий 1 |
Сценарий 2 |
Сценарий 3 |
Сценарий 4 |
|
Прогнозируемое количество переболевших, чел. |
83% населения города |
58% населения города |
21 000 |
13 000 |
|
Потребность койко-мест в больницах, шт. |
320 000 |
123 000 |
950 |
800 |
|
Потребность в аппаратах ИВЛ, шт. |
97 000 |
40 000 |
300 |
250 |
|
Прогнозируемое количество умерших. чел |
112 000 |
77 000 |
330 |
210 |
|
Ожидаемый срок пика эпидемии |
конец июня |
начало сентября |
середина апреля |
середина апреля |
|
Ожидаемый срок окончания эпидемии |
конец августа |
декабрь |
начало августа |
середина июня |
2) г. Санкт-Петербург
По аналогии было проведено моделирование распространение эпидемии на территории г. Санкт-Петербурга. Результаты представлены на рисунках 8-11.
Сценарий 1. Распространение эпидемии без каких-либо профилактических и ограничительных мероприятий.
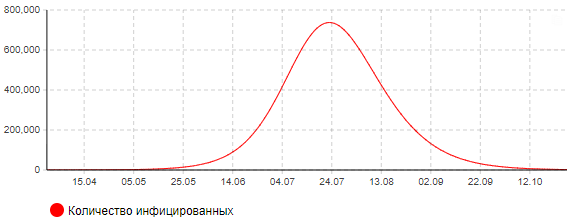
Рисунок 8а – Динамика количества инфицированных (сценарий 1)
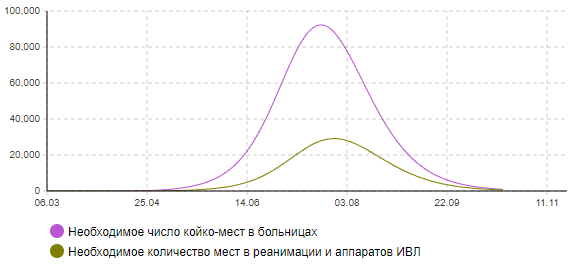
Рисунок 8б – Динамика количества тяжелых и критически больных (сценарий 1)
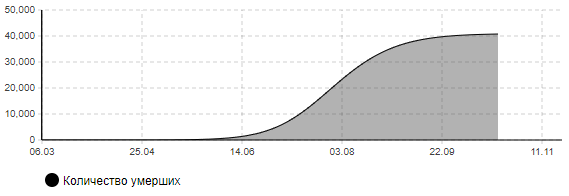
Рисунок 8в – Количество умерших (сценарий 1)
Сценарий 2. Мягкие ограничительные меры
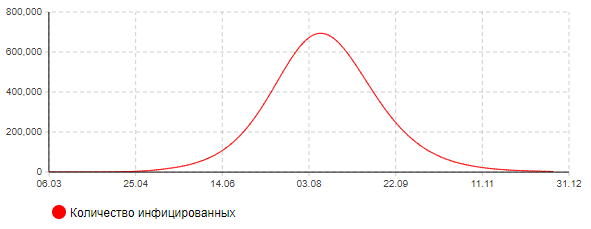
Рисунок 9а – Динамика количества инфицированных (сценарий 2)
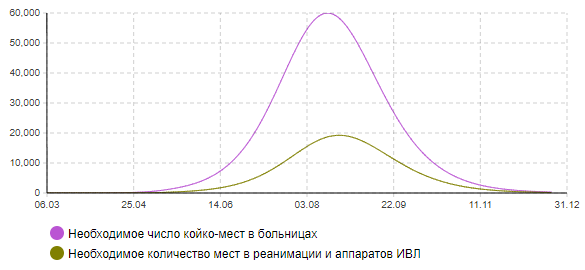
Рисунок 9б – Динамика количества тяжелых и критически больных (сценарий 2)
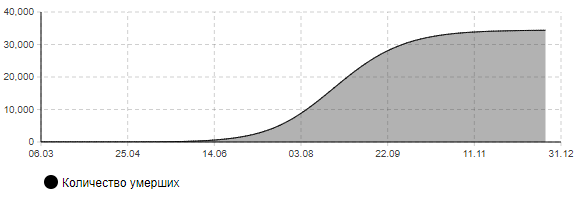
Рисунок 9в – Количество умерших (сценарий 2)
Сценарий 3. Жесткие ограничительные меры
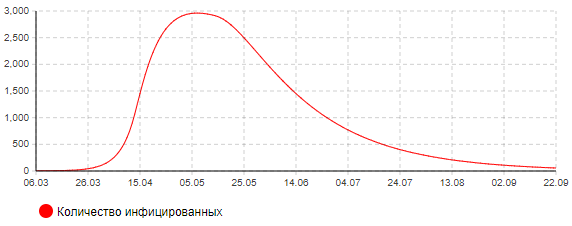
Рисунок 10а – Динамика количества инфицированных (сценарий 3)
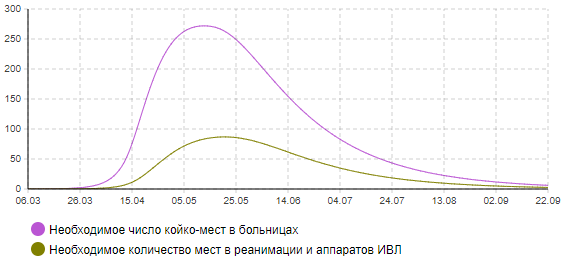
Рисунок 10б – Динамика количества тяжелых и критически больных (сценарий 3)
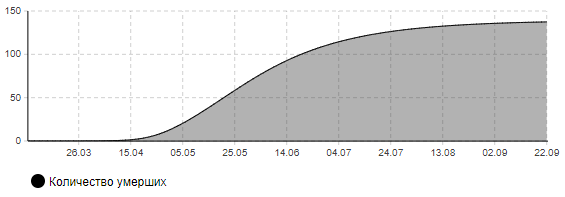
Рисунок 10в – Количество умерших (сценарий 3)
Сценарий 4. Жесткие ограничительные меры (введение карантина и режима ЧС)
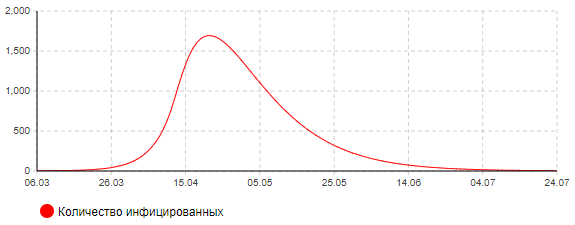
Рисунок 11а – Динамика количества инфицированных (сценарий 4)
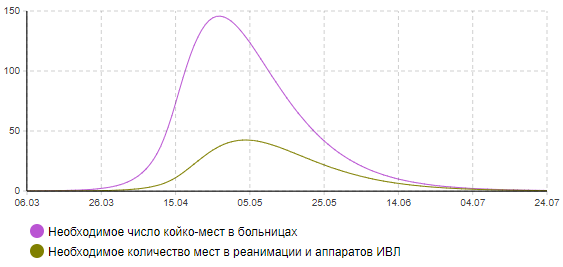
Рисунок 11б – Динамика количества тяжелых и критически больных (сценарий 4)
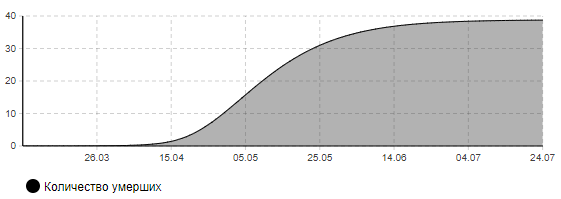
Рисунок 11в – Количество умерших (сценарий 4)
Сравнительный анализ всех рассмотренных сценариев при моделировании распространения эпидемии в г. Санкт-Петербург представлен в табл. 2.
Таблица 2.
Оценка эффективности принимаемых мер по распространению COVID-19 в г. Санкт-Петербург
|
|
Сценарий 1 |
Сценарий 2 |
Сценарий 3 |
Сценарий 4 |
|
Прогнозируемое количество переболевших, чел. |
72% населения города |
60% населения города |
8750 |
2400 |
|
Потребность койко-мест в больницах, шт. |
92 000 |
60 000 |
280 |
150 |
|
Потребность в аппаратах ИВЛ, шт. |
28 000 |
20 000 |
90 |
50 |
|
Прогнозируемое количество умерших. чел |
40 000 |
32 000 |
до 150 чел |
до 40 чел |
|
Ожидаемый срок пика эпидемии |
середина июля |
первая декада августа |
середина мая |
вторая половина апреля |
|
Ожидаемый срок окончания эпидемии |
начало сентября |
начало ноября |
середина августа |
середина июня |
Замечания и выводы
1. Необходимо отметить, что все полученные результаты весьма приблизительны. Нельзя быть уверенным в том, что даты и ход эпидемии будут соответствовать точным прогнозам, которые сделаны в данной работе. Существуют неизбежные неопределенности при прогнозировании такого явления, как эпидемия! Но полученные результаты, по крайней мере, могут вполне точно обосновать принимаемые управленческие решения, направленные на ограничения распространения эпидемии.
2. В работе предположено, что абсолютно любой человек потенциально может заразиться COVID-19, т.е. изначально нет ни одного индивидуума, обладающего полным или частичным иммунитетом, что характерно для многих других вирусных заболеваниях, «гуляющих» по планете в настоящее время. Но исследований, опровергающих данное предположение пока нет.
3. По результатам динамики роста эпидемии в течение марта месяца видно, что вводимые постепенно ограничения в целом дают положительный результат, однако оценить их эффективность можно лишь приблизительно. При моделировании предполагалось, что вводимые ограничения, которые на начальных стадиях носили сугубо рекомендательный характер, выполняются жителями в полном объеме. По факту видно, что это далеко не соответствует реальной картине, и примеров нарушения режима самоизоляции полно! В особенности это было хорошо заметно в первые, по-настоящему теплые весенние деньки. А это вполне может оказывать влияние на реальное распространение вируса, что не учитывалось в построенной модели.
Также важную роль играет время начала и период введения конкретных ограничительных мер. В данной работе были рассмотрены четыре основных сценария. Но наверняка данные сценарии в процессе реальной борьбы с распространением COVID-19 будет комбинироваться, причем последовательно с 1-го и возможно даже до 4-го в сторону постоянного их ужесточения.
4. При оценке летальности случаев заражения никак не учитывался возможный ее рост в условиях ограниченности аппаратов ИВЛ, т.е. предполагалось, что каждый больной, находящийся в критической ситуации, гарантированно сможет быть подключенным к аппарату. В этих обстоятельствах естественно предположить, что количество умерших в первых двух сценариях может оказаться существенно больше.
Также доля инфицированных, переносящих заболевание в той или иной форме, определялась весьма условно, исходя из опыта стран, столкнувшихся с ней раньше. Опыт показывает, что большая часть умерших – это люди с ослабленным иммунитетом, имеющие серьезные хронические заболевания. И их количество, конечно же, может отличаться в разных странах. Но точные данные по летальности COVID-19 в нашей страны, в любом случае, можно будет получить лишь по окончанию распространения эпидемии.
5. Результаты показывают, что период эпидемии во многом зависит от времени начала введения ограничительных мер, и она гораздо легче и быстрее подавляется при невысоком текущем количестве инфицированных. Вполне логично принятое решение руководством страны о необходимости определения степени ограничительных мер именно на уровне регионов, поскольку весьма очевидно, что ситуация с уровнем распространения эпидемии в разных регионах страны неоднородна. И если в большинстве регионов России ситуация остается еще вполне устойчивой по причине того, что ограничительные меры были введены вовремя, пока количество зараженных оценивалось единицами или десятками, то например в Москве можно было бы существенно снизить возможный ущерб, если бы, ориентируясь на сложившуюся ситуацию в других странах (в особенности Китая, Италии и пр.), ограничительные меры начались вводиться хотя бы на неделю раньше.
6. Необходимо отметить, что при первых двух сценариях переболеет больше половины населения, а значит при спаде эпидемии в случае окончания ограничительных мер не очень высокий риск начала повторной волны роста эпидемии. Третий и четвертый сценарии напротив характеризуются достаточно высоким риском начала повторной волны эпидемии, поскольку коллективного иммунитета у населения в целом к вирусу не будет, поэтому лицам, принимающим решения, необходимо будет очень взвешенно подходить к вопросу определения даты снятия всех ограничительный мероприятий.
7. Результаты показывают, что чем жестче изначально вводимые ограничительные меры, то тем меньше становится период самоизоляции населения, и тем в конечном итоге окажется слабее удар по экономике страны, которая, несомненно, будет в течение этого периода находиться в парализованном состоянии. Поскольку эпидемия развивается по траектории экспоненциального роста, то неизбежно, что руководство страны или регионов в конечном итоге будет вынуждено ввести карантин, либо официально, либо «по умолчанию». Таким образом, если это произойдет в любом случае, то стоит сделать как можно раньше!
1. World Health Organization. Coronavirus disease 2019 (COVID-19): Situation Report - 38. 27 February 2020 [Электронный ресурс]. - Режим доступа: www.who.int/docs/default-source/coronaviruse/situation-reports/20200227-sitrep-38-covid-19.pdf?sfvrsn=9f98940c_2 on 28 February 2020.
2. Инкубационный период нового коронавируса COVID-19. Сайт мониторинга коронавируса [Электронный ресурс]. - Режим доступа: https://coronavirus-monitoring.ru/2020/03/19/inkubacionnyj-period-koronavirusa-covid-19/#i-1
3. Bai Y, Yao L, Wei T, et al. Presumed Asymptomatic Carrier Transmission of COVID-19. JAMA. Published online February 21, 2020. doihttps://doi.org/10.1001/jama.2020.2565
4. Lauer SA, Grantz KH, Bi Q, et al. The Incubation Period of Coronavirus Disease 2019 (COVID-19) From Publicly Reported Confirmed Cases: Estimation and Application. Ann Intern Med. 2020; [Epub ahead of print 10 March 2020]. doi: https://doi.org/10.7326/M20-0504
5. Huang C, Wang Y, Li X, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020;395:497-506. [PMID: 31986264] doihttps://doi.org/10.1016/S0140-6736(20)30183-5
6. ВОЗ назвала процентное соотношение легкого и тяжелого течения коронавируса [Электронный ресурс]. - Режим доступа: https://gogov.ru/news/750512
7. Российский вирусолог назвал процент критических случаев при коронавирусе [Электронный ресурс]. - Режим доступа: https://lenta.ru/news/2020/04/07/ucheni/
8. Yang J. et al. Prevalence of comorbidities in the novel Wuhan coronavirus (COVID-19) infection: a systematic review and meta-analysis //International Journal of Infectious Diseases. - 2020.
9. Report of the WHO-China Joint Mission on Coronavirus Disease 2019 (COVID-19) [Электронный ресурс]. - Режим доступа: https://www.who.int/docs/default-source/coronaviruse/who-china-joint-mission-on-covid-19-final-report.pdf
10. Средний возраст заболевших коронавирусом и умерших от него. Сайт мониторинга коронавируса [Электронный ресурс]. - Режим доступа: https://coronavirus-monitoring.ru/2020/03/19/vozrast-zabolevshih-koronavirusom/
11. Report 4: Severity of 2019-novel coronavirus (nCoV) https://www.imperial.ac.uk/media/imperial-college/medicine/sph/ide/gida-fellowships/Imperial-College-COVID19-severity-10-02-2020.pdf
12. Романов Б.К. Коронавирусная инфекция COVID-2019 // Безопасность и риск фармакотерапии. - 2020. - Т. 8. - № 1. - С. 3-8.
13. Maslov S., Goldenfeld N. Window of Opportunity for Mitigation to Prevent Overflow of ICU capacity in Chicago by COVID-19 //arXiv preprint arXiv:2003.09564. - 2020.
14. Сколько дней длится заболевание COVID-19? [Электронный ресурс]. - Режим доступа: https://aif.ru/health/coronavirus/skolko_dney_dlitsya_zabolevanie_koronavirusom
15. Прилуцкий А.С. Коронавирусная болезнь 2019. Часть 1: характеристика коронавируса, эпидемиологические особенности // Вестник гигиены и эпидемиологии. - 2020. - Т. 24. - № 1. - С. 77-86.
16. Benvenuto D., Giovanetti M., Salemi M. et al. The global spread of 2019-nCoV: a molecular evolutionary analysis / // Pathog Glob Health. - 2020. - Vol. 12. - Р. 1-4. doi:https://doi.org/10.1080/20477724.2020.1725339. [Epub ahead of print]
17. Laguna M. OptQuest // Optimization of Complex Systems. - 2011.








